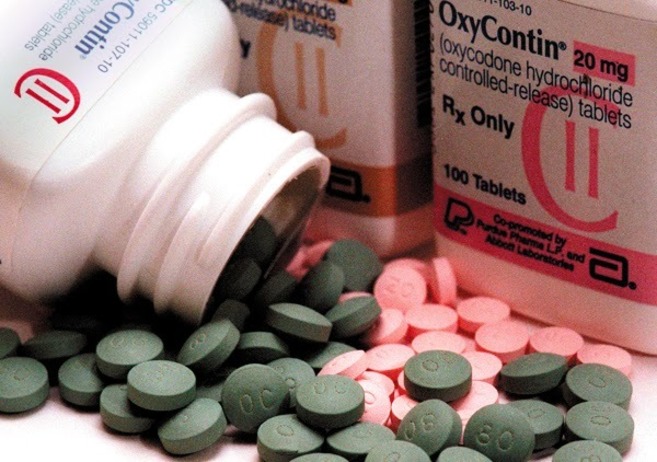
Redacción, 17-08-2015.- La Agencia Estadounidense del Medicamentoha aprobado la comercialización de una versión infantil del analgésico oxicodona (en su formulación de liberación prolongada). La nueva presentación está destinada a enfermos de entre 11 y 16 años que no respondan a otro tipo de fármacos.
Un portavoz del organismo estadounidense ha señalado que la agencia decidió aprobar el medicamento después de que la compañía productora, Purdue Pharma LP, aportara datos de ensayos clínicos sobre la seguridad y la eficacia del producto en niños. Además, afirma el periódico El Mundo, la FDA ha pedido a la farmacéutica que lleve a cabo ensayos clínicos para evaluar su uso infantil a más largo plazo.
Los médicos que tratan a menores con cáncer han alabado la nueva aprobación, mientras que otros han expresado cierta preocupación por un posible riesgo de adicción de los niños a este medicamento.
En realidad, los especialistas en Pediatría llevan años reclamando opciones analgésicas para los niños, ya que en el mercado hay muy pocas alternativas para aliviar el dolor que sean específicas para niños. Generalmente, se usan formulaciones para adultos que los especialistas intentan adaptar a las características infantiles.
Debido a este problema, la FDA pidió a la farmacéutica realizar estudios para ver si la oxicodona de liberación prolongada podía utilizarse de forma segura en niños de entre 11 y 16 años con cáncer, traumatismos o cirugías mayores, según ha afirmado Sharon Hertz, del Centro de la FDA para la Evaluación e Investigación de Fármacos.
Finalmente, la FDA ha aprobado el producto. Los médicos deberían recetar el fármaco sólo a niños que ya hayan sido tratados con analgésicos opiáceos y que puedan tolerar al menos 20 miligramos al día.